Studija zebra finka pokazuje da novonastali neuroni u odraslom mozgu mogu fizički deformisati okolne zrele ćelije i ponekad prodirati kroz njih — proces koji istraživači nazivaju „tunelovanjem“. Analiza konektoma regiona Area X identifikovala je 35 migratornih neurona u gustoj sinaptičkoj mreži, sa gustinom oko 1 390 neurona po mm³ i više od 8 miliona sinapsi u uzorku. Ponašanje može objasniti zašto sisari imaju ograničenu neurogenu sposobnost, ali i ponuditi ideje za terapije popravke mozga.
Neuroni zebrastog finka „prave tunele“ kroz mozak — novo otkriće o odrasloj neurogenezi

Zebrasti fink može stati u dlan, ali njegov mozak radi nešto neočekivano: u jednom delu odraslog mozga novonastali neuroni ne pokušavaju da se „uguraju“ između starijih ćelija, već deluju kao da guraju i deformišu okolno tkivo — ponekad čak i prave male prolaze kroz gustu mrežu zrelih neurona. To otkriće dolazi iz istraživanja tima sa Boston University i daje novi uvid u mehanizme neurogeneze kod životinja koje nastavljaju da stvaraju neurone i u odraslom dobu.
Ključni nalazi
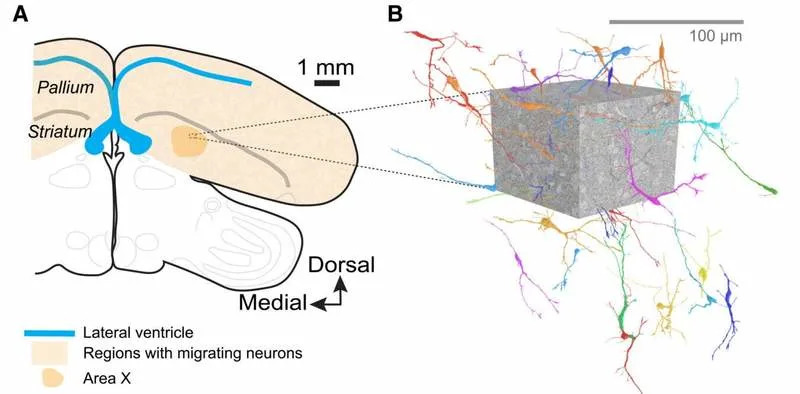
Istraživači su analizirali konektom regiona Area X, dela strijatuma povezanog sa učenjem pevanja, i identifikovali 35 migratornih neurona sa većinom kompletnih rekonstrukcija. Ti neuroni su se nalazili u gustom, sinapsama bogatom tkivu i često su bili u neposrednom kontaktu sa zrelim aksonima, dendritima i somama. U nekoliko slučajeva novoformirani neuroni su izazivali ulegnuća i savijanja kod okolnih ćelija, ponašanje koje autori nazivaju „tunelovanjem“.
Metodologija
Tim je koristio elektronsku mikroskopiju i konektomiku visoke rezolucije, uz fluorescentnu mikroskopiju i mašinsko učenje za klasifikaciju ćelijskih oblika, kako bi identifikovao i rekonstruisao migratorne neurone. Iz uzorka su izračunali gustinu migratornih ćelija i lokalnu gustinu sinapsi, a zatim su merenjima ocenili oblik i dubinu kontakata između novih i zrelih ćelija.
Podaci i brojke
- Pronađeno 35 migratornih neurona unutar snimljenog volumena.
- Procenjena gustina migratornih neurona: oko 1 390 neurona po mm³.
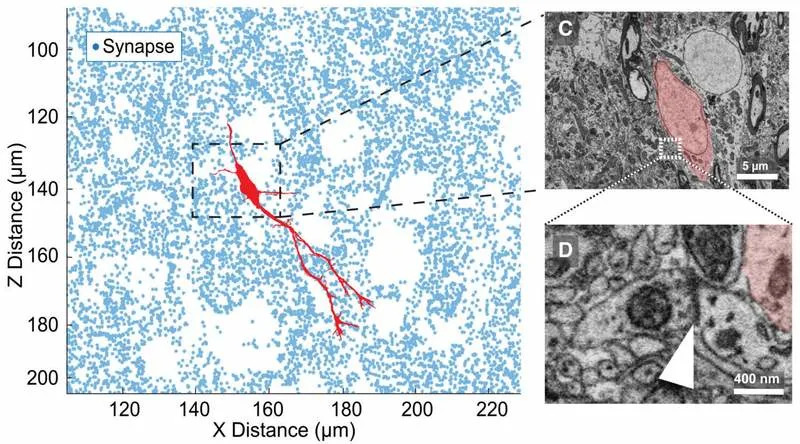
- Konektom je sadržao više od 8 miliona visokopoverljivih sinapsi; lokalna gustina sinapsi oko migratornih neurona bila je približno 0,29 po μm³.
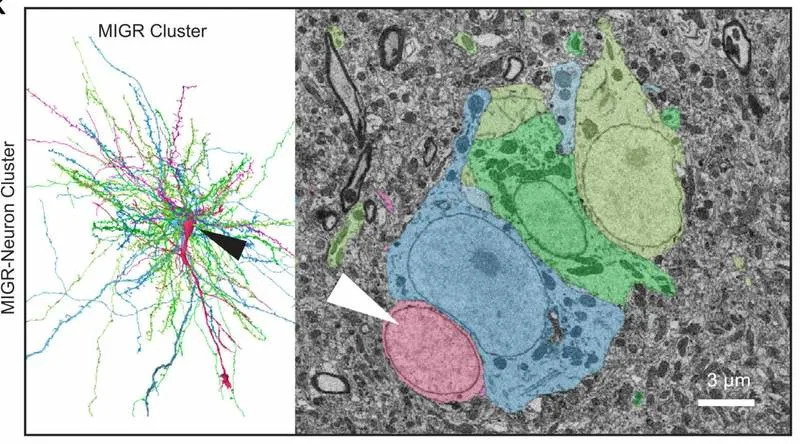
- 17 od 35 migratornih neurona formiralo je soma‑do‑soma asocijacije sa zrelim neuronima; 4 su bile u vezi sa astrocitima.
- Prosečna dubina udubljenja u telima zrelih neurona iznosila je približno 2,03 μm, naspram 0,59 μm kod migratornih ćelija.
Šta znači „tunelovanje“?
Autori pod tim terminom opisuju situacije u kojima novi neuron deluje tako da deformiše više susednih ćelija i vlakana dok se pomera kroz gusto tkivo — deluje kao da prodiru kroz skupove zrelih neurona, a ne da ih zaobilaze. To, prema istraživačima, nije ranije jasno dokumentovano u kičmenjačkom nervnom sistemu.
Implikacije
Otkriveno ponašanje postavlja pitanje troška za funkciju i memoriju: u sisara, gde su veze u mozgu stabilnije i neurogeneza ograničena posle rođenja, takvo fizičko „probijanje“ može remetiti postojeće krugove i snagu zapisanih sećanja. To može biti jedan od razloga zašto ljudi i drugi sisari imaju slabu sposobnost regeneracije odraslog mozga. S druge strane, sposobnost kretanja bez vidljivih glijalnih skafolda otvara nove ideje za strategije popravke mozga i tretmane zasnovane na matičnim ćelijama.
Ograničenja studije
Autori ističu nekoliko ograničenja: hemijska fiksacija i obrada uzoraka za elektronsku mikroskopiju mogu smanjiti ekstracelularni prostor i izmeniti dimenzije tkiva; rezolucija voxela ograničava vidljivost veoma finih struktura; greške u anotaciji ili segmentaciji mogu uticati na tumačenje; i snimani blok obuhvata ograničenu regiju Area X, nekoliko milimetara dalje od mesta rođenja neurona, pa studija možda ne prikazuje sve puteve migracije ili rane faze kretanja.
Zaključak
Studija iz Current Biology pruža konkretniji prikaz kako novonastali neuroni mogu prolaziti kroz već funkcionalan mozak kod ptica: ponekad kroz fizičku disrupciju i deformaciju okolnog tkiva. To ima važna pitanja za razumevanje učenja, pamćenja i mogućnosti popravke mozga kod ljudi.
Reference: Rad objavljen u časopisu Current Biology; istraživanje tima sa Boston University.
Pomozite nam da budemo bolji.

























