MIT‑ov tim otkrio je da običan multimodni optički kabel pri kritičnoj snazi može spontano formirati stabilan, usko fokusiran „pencil beam“ koji u multiphoton mikroskopiji omogućava 25× brže 3D snimanje humanog modela krvno‑moždane barijere uz očuvanje subćelijske rezolucije. Metoda smanjuje foto‑dozu, može se prilagoditi postojećim mikroskopima i otvara put bržem prekliničkom testiranju lekova za mozak. Potrebna su dalja istraživanja mehanizma i tehnološka usavršavanja.
MIT-ov samorganizujući laser ubrzava 3D snimanje krvno‑moždane barijere — 25× brže sa 'pencil beam' snopom

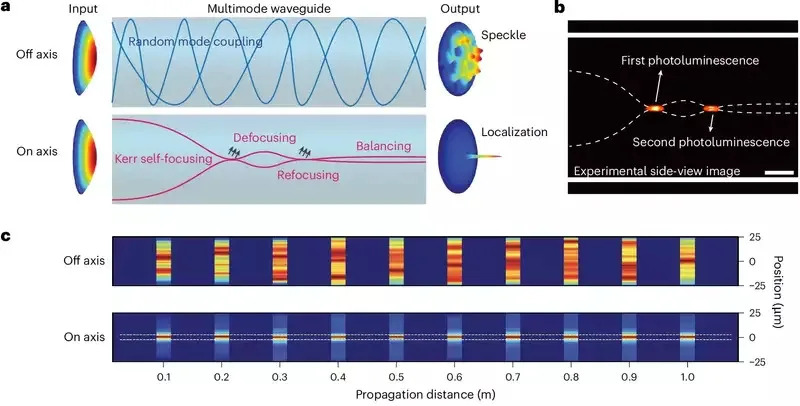
Istraživači sa MIT‑a otkrili su da visokosnažni femtosekundni laser u običnom step‑index multimodnom optičkom vlaknu može, pod strogo određenim uslovima, spontano preći iz haotičnog spekla u stabilan, usko fokusiran i samorganizovan „pencil beam“. Ovaj neočekivani režim rada omogućava brzo i visoko‑rezolutno volumetrijsko multiphoton snimanje bez komplikovanih optičkih korekcija.
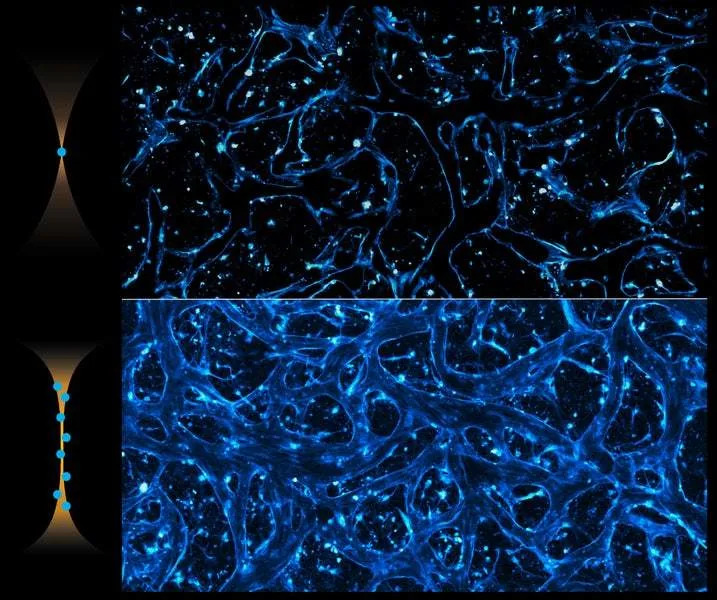
Kako su stigli do otkrića
Eksperiment je počeo kao test izdržljivosti vlakna. Kada su laser doveli blizu snage koja bi mogla da ošteti vlakno — ali ga i dalje pokrenuli tačno po osi (nulti ugao) — izlazna svetlost se, protiv očekivanja, izoštrila u centralni vrh umesto da postane još raspršenija. Tim je utvrdio da su dva uslova neophodna: precizno lansiranje snopa duž ose vlakna i dovoljna snaga da nelinearnost svetla značajno utiče na staklenu jezgru.

Tehnički detalji
- Vlakno: standardno silikonsko step‑index multimodno vlakno, prečnik jezgra 50 µm.
- Oblik snopa: lokalizovani režim sa FWHM ≈ 2,5 µm (blizu difrakcionog limita 2,3 µm).
- Pulsna dužina izlaza: ~212 fs, blizu nenedispersovanog referentnog pulsa.
- Stabilnost: relativne fluktuacije snage smanjene za ~11 dB; prostorna varijacija pri savijanju smanjena 19×.
- Granica oštećenja: ireverzibilna šteta zabeležena pri približno 5,5 MW.
Primena u biomedicinskom snimanju
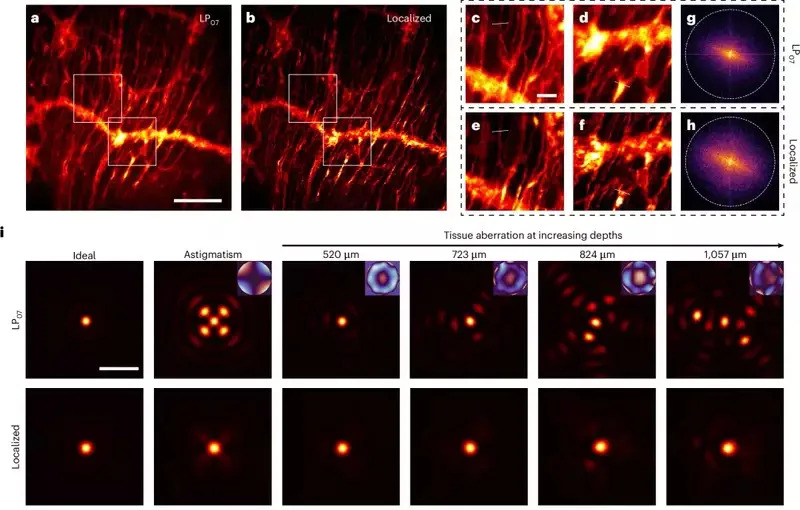
U multiphoton testovima snop je zadržao lateralnu oštrinu blisku referentnom Gaussovom snopu, dok je aksijalno produžio fokus otprilike desetostruko. U uzorku mišjeg crevnog tkiva označenog tdTomato proteinom, lokalizovani snop je proizveo jasne slike kroz prošireni aksijalni opseg u jednoj kadru, za razliku od klasičnog Gaussovog skena koji je zahtevao z‑stack od 50 µm.
Brže snimanje krvno‑moždane barijere
Tim je testirao metodu na mikrofluidnom humanom modelu krvno‑moždane barijere (endotelne ćelije izvedene iz iPSC, periciti i astrociti u fibrinskom hidrogelu), perfundirajući Alexa555‑konjugovani transferin kroz mikrovaskularnu mrežu. Lokalizovani snop je omogućio snimanje zapremine 2 mm × 2 mm × 50 µm za ~1 minut, naspram ~25 minuta potrebnih ranijim pristupima — približno 25× ubrzanje, uz očuvanje subćelijske rezolucije i nižu foto‑dozu.
Biološki uvidi
Brzo snimanje je otkrilo heterogenost u ponašanju ćelija: endotelne ćelije su u globalu dominirale transferin uptake i dosegle su plato oko 45 minuta, periciti su pokazali <30% nivoa u odnosu na endotelne ćelije, dok su astrociti imali malu ukupnu akumulaciju. Na nivou pojedinačnih ćelija, neke endotelnje ćelije internalizovale su transferin u roku od minuta, dok su susedne ćelije bile inertne. Kompetitivni test sa viškom nenaletelovanog transferina smanjio je endotelni signal ~5× posle 20 minuta, što podržava receptorno‑posredovanu endocitozu.
Prednosti i ograničenja
Prednosti: moguće retrofitting u postojeće multiphoton mikroskope, veća brzina akvizicije volumena, manja foto‑doza i visoka prostorno‑vremenska rezolucija za praćenje dinamičnih procesa u ljudskim in vitro modelima. Ograničenja: neophodna je dublja teorijska analiza mehanizma, ograničenja osetljivosti pri vizualizaciji kompletnih transcitotskih puteva, trenutna brzina snimanja vezana je za repetition rate lasera (~1 MHz) i efikasnost konverzije energije u vlaknu, a dalje povećanje snage može dovesti do trajnog oštećenja vlakna.
Objavljeno: Nature Methods. Glavni autori: Honghao Cao i Sixian You; saradnici uključuju istraživače sa MIT‑a, Harvard‑a i Beth Israel Deaconess Medical Center.
Otkriće pokazuje kako fizički fenomeni koji su nekada smatrani problemima u visokosnažnoj optici mogu postati praktični alati za brže i detaljnije posmatranje biologije u tri dimenzije i u realnom vremenu.
Pomozite nam da budemo bolji.




























