Studija Helmholtz Munich otkriva da mutacije u genu GPX4 pokreću neuronalnu smrt putem ferroptoze — procesa koji uključuje nakupljanje gvožđa i oksidativno oštećenje membrane. Rad obuhvata tri deteta sa SSMD, eksperimente na miševima i ljudske organoide, koji su pokazali isti obrazac degeneracije. Hemijsko blokiranje ferroptoze usporilo je smrt neurona u modelima, sugerišući moguću vezu sa čestim neurodegenerativnim bolestima.
Retka Mutacija GPX4 Uništava Neurone Kroz Ferroptozu — Naučnici Razotkrili Mehanizam

Eksperimenti na ultra-retkoj genetskoj mutaciji koja izaziva tešku neurodegeneraciju kod dece otkrili su novi mehanizam kojim moždane ćelije umiru — i otvorili put ka razumevanju sličnih procesa u čestim bolestima poput Alchajmera, Parkinsona i Hantingtonove bolesti.
Tim istraživača iz nemačkog centra Helmholtz Munich utvrdio je da mutacije u genu GPX4 dovode do progresivne inflamacije i odumiranja neurona kod miševa. Laboratorijski uzgojeni ljudski neuroni i mini‑mozgovi (organoidi), dobijeni iz kožnih ćelija pacijenata sa istom mutacijom, pokazali su istovetan obrazac degeneracije.
Specifičan oblik programirane ćelijske smrti koji je identifikovan zove se ferroptoza — proces koji aktivira nagomilavanje gvožđa i oksidativno oštećenje lipidnog dela ćelijske membrane.
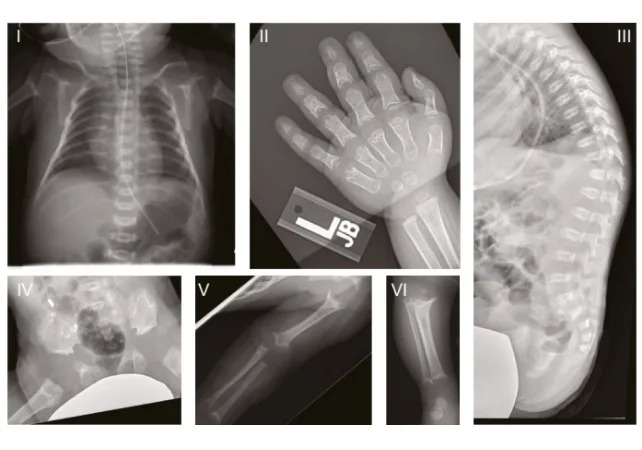
Istraživanje se fokusiralo na troje dece iz SAD sa dijagnozom Sedaghatian‑type spondylometaphyseal dysplasia (SSMD), koja su imala mutacije u istoj funkcionalnoj regiji GPX4. Nalazi iz kliničkih uzoraka upotrebljeni su za eksperimente na modelima kod miševa i u ljudskim ćelijskim kulturama, što je potvrdilo konzistentan mehanizam smrtnog puta neurona.
Marcus Conrad, direktor Instituta za metabolizam i ćelijsku smrt u Helmholtz Munich, poredi enzim GPX4 sa surf daskom:
"Sa perajom uronjenom u membranu, GPX4 klizi duž unutrašnje površine i brzo razgrađuje lipidne perokside — štiteći membrane neurona."
Međutim, kod određene mutacije fin (peraja) enzima nedostaje, pa GPX4 više nije ukotvljen u membranu i ne može da obavlja svoju zaštitnu ulogu. Neuroni tako postaju posebno osetljivi na ferroptozu.

Istraživači su takođe pokazali da hemijsko blokiranje ferroptoze u modelima — i kod miševa i u ćelijskim kulturama — usporava gubitak neurona, što sugeriše da je ferroptoza pokretačka snaga u ovom obliku neurodegeneracije, a ne samo prateći efekat.
Svenja Lorenz iz Helmholtz Municha ističe da dosadašnja istraživanja demencije često naglašavaju taloženje proteina (npr. amiloid‑β), dok ovi rezultati preusmeravaju pažnju i na oštećenje ćelijske membrane kao rani i ključni događaj.
Autori napominju da, iako mutacije u GPX4 izazivaju retki SSMD i ne znače automatski rani početak uobičajenih oblika demencije, razumevanje ovog puta ćelijske smrti može pomoći u otkrivanju novih terapijskih pristupa i za češće neurodegenerativne bolesti.
Studija je objavljena u časopisu Cell. Autori pozivaju na nastavak osnovnog istraživanja i dugoročno finansiranje kako bi se dalje razjasnili mehanizmi i razvile potencijalne terapije.
Pomozite nam da budemo bolji.























