Nova studija otkriva da MPS — ponavljajuća rešetka od aktina i spektina ispod neuronske membrane — deluje kao fizički "vratar" koji ograničava endocitozu i time kontroliše signalizaciju. Smanjenje βII-spektrina (~70%) ubrzava sve glavne endocitne puteve i skraćuje vreme internalizacije transferrina, LDL-a i APP-a. Endocitoza aktivira ERK, koji pokreće proteaze (pre svega kalpain), cepa spektin i dodatno slabi MPS, stvarajući pozitivnu povratnu petlju koja povećava Aβ42 akumulaciju u neuronima s povećanom ekspresijom APP-a. Očuvanje MPS-a može predstavljati novi pravac za terapiju Alchajmerove bolesti, uz potrebu za daljim in vivo istraživanjima.
„Vratar” Ispod Membrane: Kako Rešetka Neurona Može Smanjiti Rizik Od Alchajmera

Neuroni su stalno u pokretu: receptori ulaze i izlaze sa površine ćelije, signali brzo rastu i opadaju, a ispod membrane leži fina rešetka od aktina i spektina koja utiče na to šta ćelija dopušta unutra. Novo istraživanje pokazuje da ta struktura — poznata kao membrane-associated periodic skeleton (MPS) — funkcioniše kao fizički „vratar” koji ograničava endocitozu i time kontroliše intenzitet i trajanje signalizacije.
Šta su naučnici otkrili
Istraživači su pomoću superrezolucione mikroskopije mapirali četiri velike endocitne rute u zrelim neuronima: klatrin-posredovanu, caveolin-posredovanu, flotilin-posredovanu i brzu endofilin-posredovanu

Pitovi su u proseku imali dimenzije: klatrin ≈ 82 nm, caveolin ≈ 75 nm, flotilin ≈ 72 nm i endofilin ≈ 67 nm. Razmak prstenastih elemenata MPS-a bio je oko 190 nm duž neurita.
Funkcija MPS-a kao kočnice endocitoze
Da bi proverili ulogu rešetke, tim je smanjio nivo βII-spektrina za ~70% u zrelim neuronima. Nakon narušavanja MPS-a porasla je gustina endocitnih udubina u aksonima i dendritima, a sve četiri rute su bili ubrzane. U modelima gde dendritični MPS nije potpuno formiran (nezrele kulture), smanjenje βII-spektrina nije imalo isti efekat, što ukazuje da je sam skafold ključan za kočenje endocitoze.
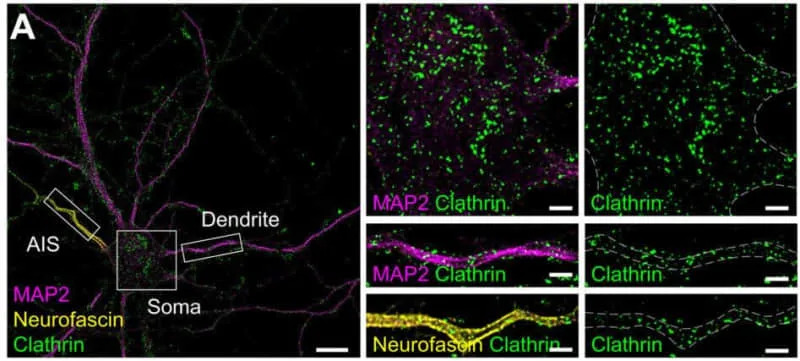
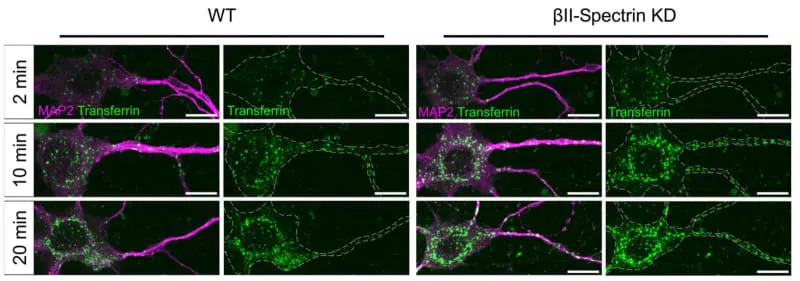
Ligandno inducirana internalizacija takođe je bila brža: transferrin — konstanta vremena smanjena je sa 17,15 na 8,29 min, LDL sa 54,63 na 35,25 min, a internalizacija HA-mGluR5a (caveolin-povezana) sa 37,77 na 9,18 min nakon slabljenja MPS-a. Internalizacija APP-a se ubrzala sa 37,21 na 14,52 minuta.
Povratna petlja koja pojačava preuzimanje
Endocitoza pokreće ERK signalizaciju; unutrašnji receptori doprinose trajanju ERK aktivacije. ERK aktivacija je bila povezana sa razgradnjom MPS-a: inhibicija ERK-a (U0126) ili blokada endocitoze (dyngo-4a) sprečavali su tu degradaciju. Dalje, inhibitiranje proteaza — naročito kalpaina (MDL-28170) i kaspaza (Z-VAD-FMK) — sačuvalo je integritet spektina. Western blot je pokazao fragmente kompatibilne sa kalpainom.
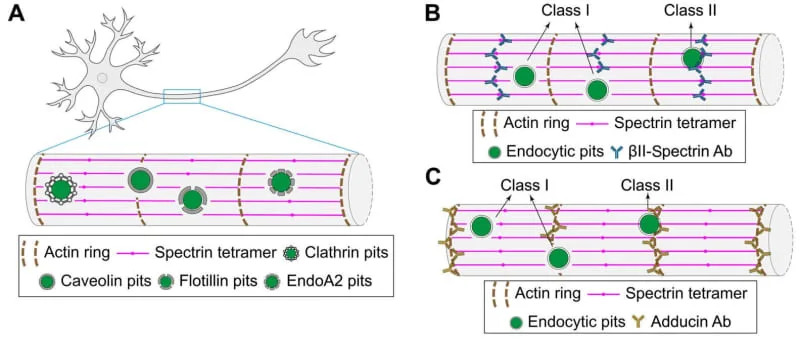
Podaci podržavaju pozitivnu povratnu petlju: endocitoza → ERK aktivacija → aktivacija proteaza (kalpain/kaspaze) → cepanje spektina → slabljenje MPS-a → još brža endocitoza. To omogućava brzu eskalaciju odgovora, ali i potencijalnu ranjivost tokom starenja ili stresa.
Povezanost sa APP i Aβ42
U neuronima koji prekomerno eksprimiraju APP695 (WT ili Swedish mutacija), narušavanje MPS-a povećava intracelularnu akumulaciju patogenog Aβ42 i aktivaciju prekomerno cleaviranog kaspaza-3, dok bez prekomerne ekspresije APP-a βII-spektrin knockdown sam po sebi nije povećao Aβ42. To ukazuje da MPS ograničava internalizaciju APP-a i posredovano formiranje Aβ42.
Implikacije i oprez
Rad ukazuje na MPS kao dinamički regulator membrane koji može predstavljati novi cilj za terapijske strategije: stabilizacija MPS-a ili prekidanje patogene povratne petlje (npr. ciljane inhibicije kalpaina/kaspaza ili modulatora ERK-a) mogli bi smanjiti prekomernu internalizaciju APP-a bez potpunog blokiranja potrebne signalizacije. Međutim, rezultati su dobijeni u kulturi neurona i zahtevaju dalja istraživanja u in vivo modelima pre nego što se razmišljanja o terapiji mogu direktno primeniti na ljude.
Studija je objavljena u časopisu Science Advances.
Pomozite nam da budemo bolji.