Kanadski tim je razvio trodimenzionalno kucajuće "srce na čipu" koje koristi dvoslojni senzorski sistem za merenje kontrakcija i lokalnih ćelijskih sila. Uređaj kombinuje elastične stubiće za makro-merenja i hidrogel kapljice (~50 µm) za mikromehanička očitavanja. Testovi sa norepinefrinom i blebbistatinom pokazali su predvidive efekte, što potvrđuje potencijal platforme za farmakološko presejavanje i personalizovanu medicinu.
Kucajuće "srce na čipu" Donosi Proboj — Korak Ka Personalizovanoj Medicini

Naučnici iz Kanade razvili su trodimenzionalni model koji oponaša otkucaje srca i meri mehaničku aktivnost od nivoa pojedinačnih ćelija do celog tkiva. Taj sistem, poznat kao kucajuće "srce na čipu" (HOC), integriše dvoslojni senzorski pristup koji omogućava praćenje u realnom vremenu i visokorezolutno merenje ćelijske funkcije.
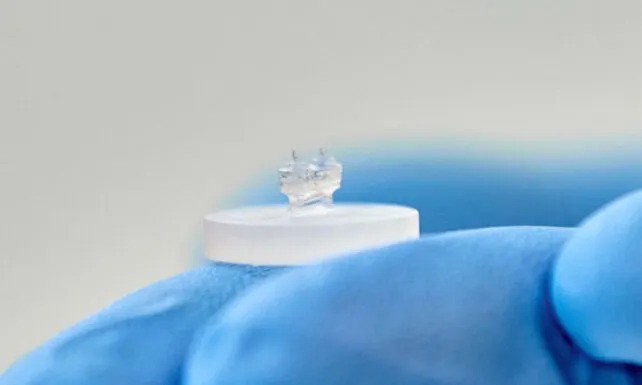
Kako funkcioniše uređaj
Istraživači su uzeli kardiomiocite i ćelije vezivnog tkiva iz pacova, ugradili ih u gelastu matricu bogatu fibrozanim proteinima i posejali na savitljive silicijumske čipove. Inženjersko srčano tkivo spontano kuca, koristeći mobilizaciju kalcijuma za iniciranje kontrakcija, što ga čini podobnim za proučavanje fizioloških i patoloških stanja.

Dvoslojni senzorski sistem
Makro-senzori: Tkivo je postavljeno između dve elastične kapije (stubova) koje se deformišu pri svakom otkucaju; ta deformacija odražava ukupnu kontraktilnu snagu kroz celo tkivo.

Mikro-senzori: U samu masu tkiva su umešane fleksibilne hidrogel kapljice prečnika ~50 mikrometara koje detektuju lokalne mehaničke napone na nivou pojedinačnih ćelija. Ova kombinacija omogućava paralelno praćenje globalne i ćelijske funkcije srca.
Farmakološko testiranje i validacija
Da bi proverili upotrebljivost platforme za testiranje lekova, tim je primenio dva dobro poznata jedinjenja: norepinefrin (noradrenalin), koji pojačava srčanu aktivnost, i blebbistatin, inhibitor mišićne kontrakcije. HOC je odgovorio predvidljivo—povećanjem odnosno smanjenjem kontraktilnih sila—pokazujući potencijal za predkliničko presejavanje i procenu farmakodinamičkih efekata.
Ali Mousavi, prvi autor iz Univerziteta u Montrealu: "Mogućnost praćenja reakcije tkiva u realnom vremenu predstavlja veliku prednost za predklinički razvoj i translaciona istraživanja."
Primenjivost i naredni koraci
Tim planira da naredne modele gradi od ćelija pacijenata sa specifičnim srčanim oboljenjima, kao što su dilatirana kardiomiopatija i različite aritmije. Cilj je razviti personalizovane testove koji bi pomogli lekarima da izaberu najučinkovitiju terapiju pre primene kod pacijenta.
Rad je objavljen u časopisu Nano Micro Small. Ovaj pristup može ubrzati prevođenje laboratorijskih nalaza u kliničku praksu i unaprediti preciznu medicinu, ali su potrebne dalje studije koje će uključiti ljudske ćelije i rigorozniju validaciju.
Houman Savoji, stariji autor: "Ovaj proboj nas približava pravoj preciznoj medicini — omogućava identifikaciju najefikasnijih lekova za svaku osobu pre nego što lečenje počne."
Pomozite nam da budemo bolji.