Tim sa ETH Zurich razvio je mekani hidrogel (97% vode, 3% polimera) koji se dvofotonim laserskim pisanjem može štampati u koštolike mikrostrukture pri rekordnoj brzini do 400 mm/s i rezoluciji oko 500 nm. Novi makromolekularni prekriživač PVASH poboljšava štampivost i stabilnost pri niskim koncentracijama polimera, dok su mehanička svojstva u opsegu 0,1–10 kPa. In vitro testovi pokazuju visoku ćelijsku vitalnost (>95%), a sledeći korak su preklinička testiranja na životinjama.
Novi hidrogel sa mikroporoznom strukturom štampa koštane implante rekordnom brzinom

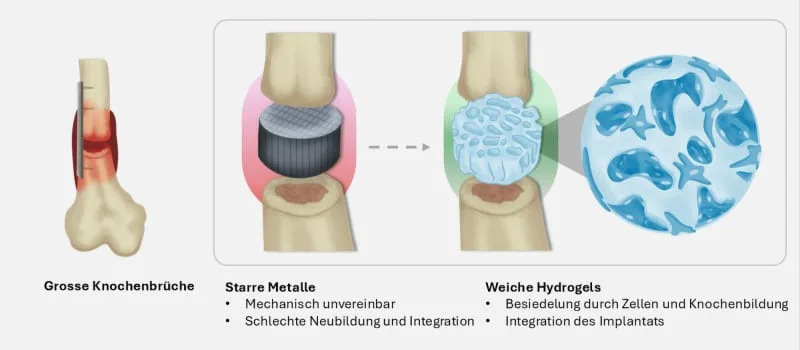
Komad zdrave kosti nije homogen čvrst blok: u njemu postoji složena mreža sitnih kanala kroz koje protiče tečnost i kojima ćelije migriraju, dobijaju nutrijente i obnavljaju tkivo. Istraživači sa ETH Zurich razvili su mekani hidrogel koji se laserski može „štampati" u takve koštolike mikroarhitekture pri rekordnoj brzini do 400 mm/s, uz finu rezoluciju od ~500 nm.
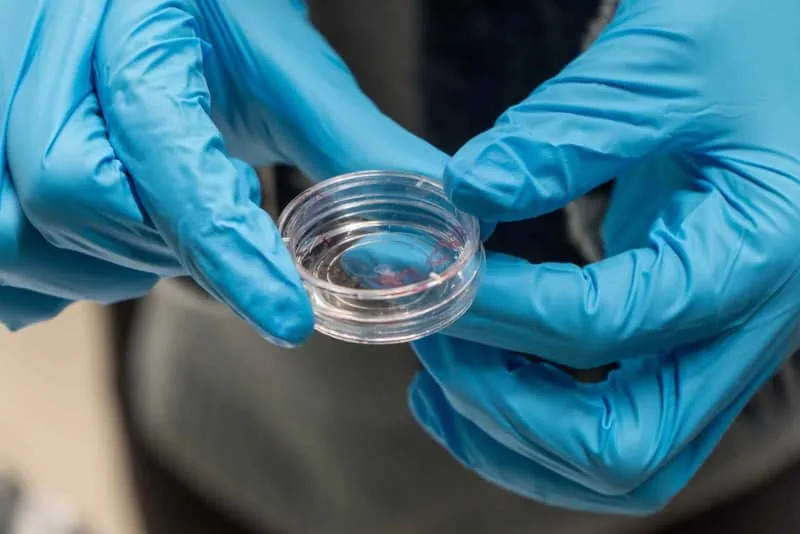
Kako funkcioniše hidrogel
Hidrogel se sastoji od 97% vode i 3% biokompatibilnog polimera (norbornen-funkcionalizovan PVA, nPVA). Ključ je u novom makromolekularnom tiol prekriživaču PVASH i u fotosenzitivnim molekulama koje aktiviraju povezivanje polimera na izloženim mestima svetlosti. Kratki laserski impulsi pokreću dvofotonapolimerizaciju (2PP), što omogućava očvršćavanje samo u veoma malom, ciljnom volumenu. Neosvetljeni gel se zatim ispere i ostaju željene 3D strukture.

Tehnički doprinosi
Glavne prednosti pristupa ETH tima su:
- Visoka brzina pisanja: do 400 mm/s (istraživači navode kao novi svetski rekord za ovaj pristup).
- Fina rezolucija: strukture do ~500 nm.
- Poboljšana štampivost pri niskim koncentracijama polimera: zahvaljujući PVASH prekriživaču smanjuju se intramolekularne „petlje" koje slabe mrežu, pa se postižu stabilniji gelovi pri 2–4% polimera u formulaciji.
Mehanička svojstva i degradacija
U mehaničkim i testovima bubrenja tim je zabeležio vrednosti skladišnog modula (storage modulus) u opsegu od približno 0,1 do 10 kPa zavisno od koncentracije, što je u domenu mekoće vanćelijskog matriksa. Degradacija je snažno zavisila od pH: pri pH 10 gelovi su izgubili strukturu i potpuno degradirali za ~14 dana, dok su pri fiziološkom pH 7,4 pokazali znatno umereniju degradaciju i očuvanu oblikovnu vernost.

Štampanje niskog sadržaja polimera i strategije stabilizacije
Dok konvencionalni 2PP pristupi često koriste 20–50% polimera za pouzdanu štampu, PVASH omogućava šire procesno „prozorsko" područje pri 3–4% polimera. Pri 2% štampivost opada zbog nedovoljne gustine prekrižavanja, ali autori su demonstrirali poboljšanje dodavanjem 3% želatina kao privremene (žrtvene) mreže — većina želatina difunduје iz strukture nakon inkubacije, dok štampani objekti ostaju stabilni na 37 °C nekoliko dana.
Ćelijski testovi i biofunkcionalizacija
U in vitro testovima PVASH makromer rastvori su pokazali visoku ćelijsku vitalnost (>95% nakon 24 h, MTS test) sa ljudskim dermalnim fibroblastima. Za prianjanje ćelija na mikro-skafolde korišćeni su RGD-peptidni motivi prikačeni na nPVA; bez RGD ćelije se nisu vezivale. Na woodpile skafoldima sa porama od 10 µm fibroblasti su se raširili i formirali protru zije, dok su veće pore od 25 µm zadržavale manje ćelija — verovatno zbog sedimentacije.
Sledeći koraci
Rad je još uvek u laboratorijskoj fazi: slede preklinička ispitivanja na životinjama u saradnji sa AO Research Institute Davos kako bi se proverilo privlačenje osteogenih ćelija in vivo i doprinos obnove mehaničke čvrstoće kosti tokom vremena. Autori takođe ističu otvorena pitanja: kvantitativna konverzija tiol grupa nakon 2PP, mehanobiološki aspekti interakcije ćelija i dugoročna biokompatibilnost i biorazgradnja.
Zaključak: Materijal koji počinje mekan, moguće se štampa u kompleksnu koštanu mikroarhitekturu i postepeno se razgrađuje mogao bi promeniti koncept implanta — od rigidnog „zamenskom dela" ka skafoldu koji aktivno omogućava i usmerava regeneraciju tkiva.
Izvor: rad objavljen u časopisu Advanced Materials. Autori navode da su rezultati ograničeni na in vitro eksperimente i da su potrebne daljnje studije pre kliničke primene.
Pomozite nam da budemo bolji.




























