Studija objavljena 7. januara u Nature pokazuje da satelitske glijalne ćelije mogu da prenose mitohondrije u perifernе neurone putem tunneling nanotubesa, vezikula i membranskih kanala. Ometanje tog prenosa u miševima dovodi do oštećenja nerava i pojačanog bola, dok prenos zdravih glija ublažava simptome. Nalazi otvaraju mogućnosti terapija koje ciljaju obnovu mitohondrijske razmene, ali su potrebne dodatne studije pre kliničke primene.
Rani podaci: Prenos mitohondrija u nerve mogao bi ublažiti hronični neuropatski bol

Novo istraživanje sugeriše da satelitske glijalne ćelije mogu da prenose mitohondrije u periferne neurone i tako održavaju njihovu energetsku funkciju — što otvara potencijalne puteve za lečenje hroničnog neuropatskog bola. Studija, objavljena 7. januara u časopisu Nature, obuhvatila je eksperimente na ćelijskim kulturama, miševima i ljudskom tkivu.
Šta su istraživači otkrili
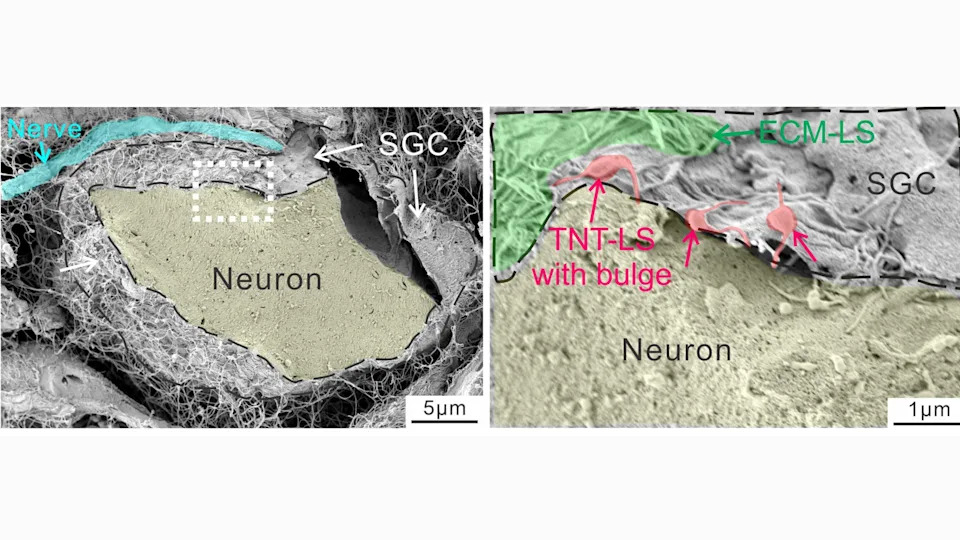
Tim na čelu sa dr Ru‑Rong Ji sa Duke University otkrio je da satelitske glijalne ćelije koje obavijaju telа perifernih neurona mogu da isporuče mitohondrije u same neurone. Ovaj prenos se odvija kroz prolazne kanale poznate kao tunneling nanotubes, ali i putem malih vezikula ili specijalizovanih membranskih kanala.

Kako to utiče na bol
U eksperimenatima na zdravim laboratorijskim miševima, ometanje prenosa mitohondrija dovodilo je do oštećenja nervnih vlakana i povećane osetljivosti na bol, jer neuroni bez dovoljno energije počnu da ispaljuju impulse nenamerno. U modelima neuropatije izazvane hemoterapijom i dijabetesom, razmena mitohondrija bila je narušena — prenosi zdravih glijalnih ćelija ublažili su bolne simptome u tim životinjama.
Mehanizmi prenosa i molekularni akteri
Istraživači su vizualizovali "izbočine" u nanotubusima koje ukazuju na transport materijala i pratili mitohondrije pomoću fluorescentnih markera. Protein MYO10 identifikovan je kao ključan za formiranje tih nanotubusa. Autorima studije je takođe zapaženo da veća nervna vlakna dobijaju više mitohondrija iz glija nego mala vlakna, što može objasniti veću ranjivost tankih vlakana kod dijabetesa i posle hemoterapije.
Terapeutske mogućnosti i ograničenja
Na osnovu nalaza, autori predlažu dva moguća pristupa: pojačavanje sposobnosti satelitskih glijalnih ćelija da proizvode i isporučuju mitohondrije, ili izolacija i primena laboratorijski uzgojenih mitohondrija direktno u oštećene nerve. Ipak, važno je naglasiti da su ovo preklinički podaci — većina rezultata dolazi iz studija na životinjama i tkivima izvan organizma; potrebne su dalje studije pre nego što se predlozi mogu primeniti na ljude.
„Ako neuron stalno prekomerno ispaljuje impulse, na kraju će verovatno degenerisati,” rekao je dr Ru‑Rong Ji, ističući kako poremećaj energetskog snabdevanja može dugoročno dovesti do neurodegeneracije.
Zaključak
Studija otkriva važnu ulogu glije u održavanju funkcije perifernih neurona i otvara nove pravce za istraživanje tretmana neuropatskog bola. Međutim, prelazak od laboratorijskih nalaza do sigurnih i efikasnih terapija za ljude zahteva dodatne kliničke studije i procenu bezbednosti.
Izvor: Nature (7. januar), izjave istraživača i podaci iz eksperimenata na miševima, ćelijskim kulturama i ljudskom tkivu.
Pomozite nam da budemo bolji.