Stanford tim je razvio intranazalnu formulaciju (GLA‑3M‑052‑LS + OVA) koja kod miševa pruža višemesečnu zaštitu protiv različitih respiratornih izazova — virusa, bolničkih bakterija i alergena. Efekat je vezan za dugotrajne plućne T‑ćelije i reprogramirane alveolarne makrofage, a potkrepljen je zavisnošću od CD4+ i CD8+ T‑ćelija i RANKL signala. Rezultati su obećavajući, ali su potrebna klinička ispitivanja u ljudi zbog razlika između miševa i ljudskog mukozalnog imunog iskustva.
Nova nosna vakcina u miševa štiti pluća mesecima — protiv virusa, bolničkih bakterija i alergena

Tim istraživača sa Stanford Medicine razvio je intranazalnu (nosnu) formulaciju koja je kod miševa pružala višemesečnu zaštitu protiv više respiratornih pretnji — uključujući SARS‑CoV‑2, neke sojeve majske SARS sojeve (MA15), bolničke bakterije i čak alergene povezane sa astmom. Rad je objavljen u časopisu Science.

Šta je novo u pristupu
Za razliku od većine vakcina koje ciljaju specifične antigene patogena, ova formulacija (označena kao GLA‑3M‑052‑LS + OVA) ne imitira konkretan virus ili bakteriju. Kombinuje dva TLR agonista — GLA (TLR4) i 3M‑052‑LS (TLR7/8) — sa bezopasnim antigenom ovalbuminom (OVA). Ideja je da TLR agonisti daju snažan „signal opasnosti“ za urođene ćelije, dok OVA pomaže da se T‑ćelije regrutuju i zatoče u plućnom tkivu, čime se produžava efekt.
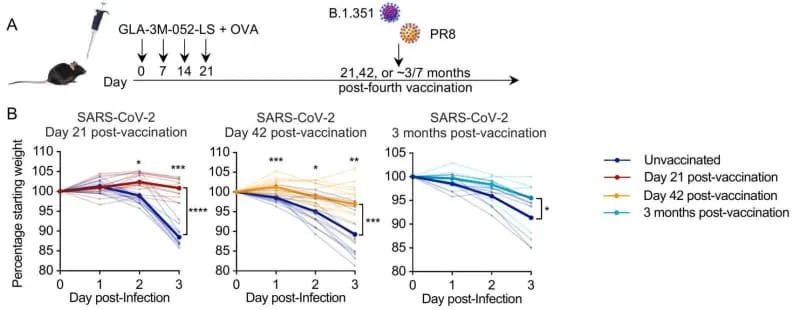
Rezultati u modelu na miševima
Istraživači su primenili intranazalnu vakcinaciju po šemi od tri do četiri doze. Nakon toga su miševe izazivali različitim respiratornim pretnjama u više vremenskih tačaka — uključujući 21 dan, 42 dana i oko tri meseca posle imunizacije.
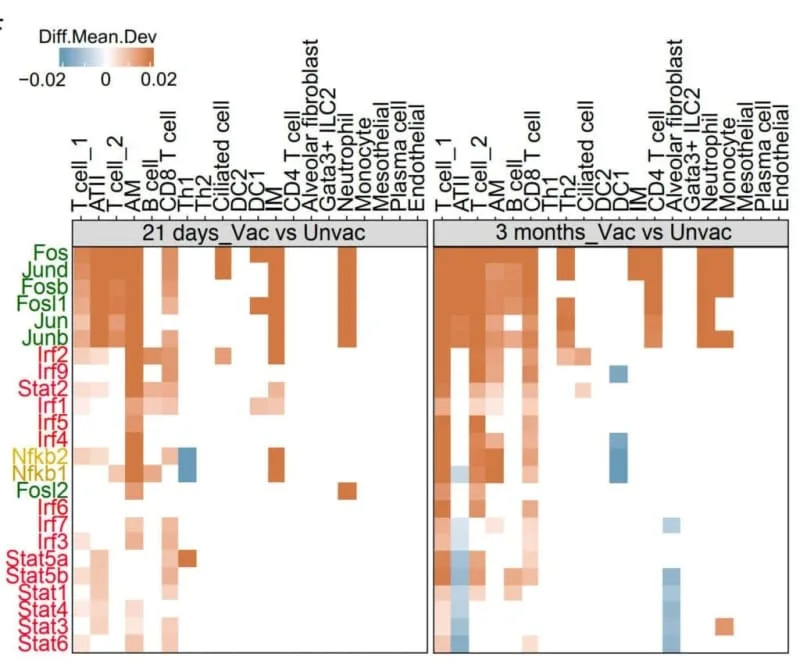
Glavni nalazi:
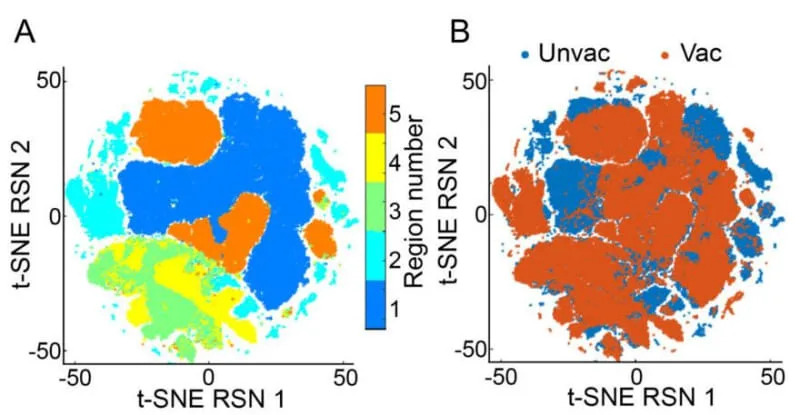
- Pri izazovu SARS‑CoV‑2 vakcinisani miševi su imali znatno manji gubitak težine, niži virusni teret u plućima i manje upale i oštećenja plućnog tkiva, i to i do tri meseca nakon vakcinacije.
- Prijavljena je delimična unakrsna zaštita i protiv SARS‑CoV MA15 i SCH014 MA15 sojeva.
- Vakcina je smanjila bakterijsko opterećenje u plućima nakon izazova sa Staphylococcus aureus i Acinetobacter baumannii, uključujući merenja oko tri meseca posle imunizacije. Takođe je prijavljeno smanjenje bakterijskog opterećenja u bubrezima pri intravenskom izazovu S. aureus.
- U modelu astme izazvane grinjem iz kućne prašine vakcinisani miševi su pokazali slabiji Th2‑alergijski odgovor, niži serumski IgE i manje stvaranja sluzi u disajnim putevima, s efektom koji je trajao najmanje tri meseca.
Mehanizmi i zavisnosti
Studija ukazuje na kombinovani odgovor: dugotrajne antigen‑specifične T‑ćelije u plućima (uključujući tkivno‑residentne memorijske T‑ćelije) i trajne promene u alveolarnim makrofagima koji deluju reprogramirano. Autori konceptualizuju ovo kao "integrisani imunitet organa", gde urođene ćelije, adaptivne T‑ćelije i strukturne ćelije pluća deluju koordinisano.
Eksperimenti su pokazali da uklanjanje oba CD4+ i CD8+ T‑ćelija tokom imunizacije uklanja zaštitu protiv SARS‑CoV‑2 i protiv bakterijskog opterećenja S. aureus. Dalje, blokada RANKL tokom imunizacija ukidala je zaštitu, dok farmakološka inhibicija CD40L, IFN‑γ ili TNF‑α nije imala isti efekat u testiranim izazovima.
Ograničenja i sledeći koraci
Autori jasno naglašavaju da su rezultati dobijeni na miševima i da direktno prenošenje na ljude nije zagarantovano. Mukozalni imunitet kod ljudi oblikovan je dugoročnim izlaganjima, vakcinacijama i infekcijama tokom života, što može uticati na odgovor. Potrebne su pažljivo kontrolisane studije na ljudima, a moguće su i bezbednosne i efikasnosne razlike u odnosu na modele na miševima.
Zaključak
Studija predstavlja konceptualno nov pristup: umesto da se cilja jedan specifičan patogen, cilj je postaviti plućni imuni sistem u produženo stanje pripravnosti pomoću kombinacije TLR stimulacije i antigen‑zavisne T‑ćelijske podrške. Rezultati su obećavajući u prekliničnom modelu, ali neophodni su dalji eksperimenti i klinička ispitivanja da bi se procenila primena kod ljudi.
Izvor: Stanford Medicine; istraživanje objavljeno u Science. Autori studije: Bali Pulendran i saradnici; vodeći autor: Haibo Zhang.
Pomozite nam da budemo bolji.



























