MIT tim je razvio injektabilne „satelitske jetre“ — male GelMA niše sa ljudskim hepatocitima i fibroblastima koje se ubrizgavaju ultrazvukom. U NSG miševima, graftovi sa mikrosferama (~110 µm) ostali su lokalizovani, vaskularizovani i proizvodili ljudski albumin do osme nedelje. Ključ uspeha su GelMA mikrosfere koje čuvaju praznine za vaskularizaciju, ultrazvučno vođeno ubrizgavanje i podrška fibroblasta; glavni izazovi su skaliranje, imuni odgovor i praćenje komponenti.
MIT Razvio Injektabilne „Satelitske Jetre“ — Mala Niša Koja Može Dati Dodatnu Funkciju Jetre

Više od 10.000 Amerikanaca čeka transplantaciju jetre, dok mnogi pacijenti ne uđu na listu jer su previše bolesni za velike operacije. Tim sa MIT‑a razvija alternativni pristup: male, injektabilne „satelitske jetre“ — lokalizovane niše koje sadrže hepatocite i pomoćne ćelije u hidrogelu, a koje mogu delimično preuzeti funkcije jetre dok bolesni organ ostane na mestu.
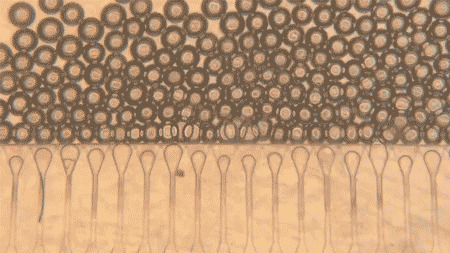
Šta su „satelitske jetre“?
Autori, na čelu sa prof. Sangeetom Bhatiom i vodećim autorom Vardhmanom Kumarom, opisali su koncept kao gotovu, injektabilnu ćelijsku nišu. Sistem kombinuje primarne ljudske hepatocite, neonatalne humane dermalne fibroblaste i mikrosfere od gelatin methacryloyl (GelMA). Mikrosfere imaju prosek od oko 110 µm i mogu se gusto spakovati tako da kroz iglu tečno prolaze, a nakon ubrizgavanja ponovo formiraju stabilnu strukturu sa međuprostorima za vaskularizaciju.
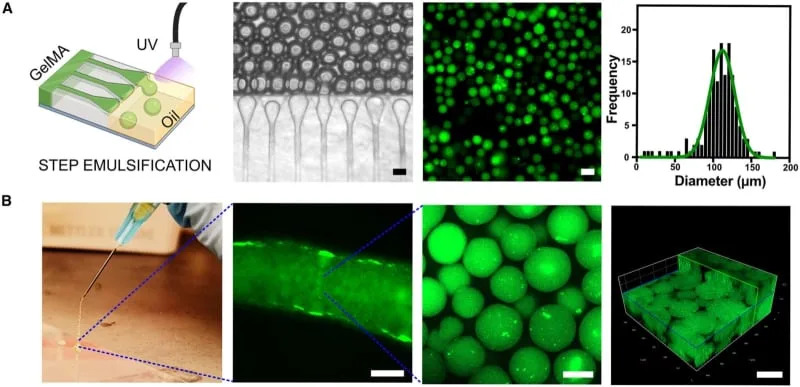
Ključni eksperimentalni nalazi
- U modelu NSG miševa, graftovi koji sadrže GelMA mikrosfere ostali su lokalizovani i detektabilni ultrazvukom tokom cele osmonedeljne studije, dok su agregati bez mikrosfera raspršeni i nestali.
- Graftovi sa mikrosferama su bili vaskularizovani: krvni sudovi su infiltrirali prostore između sfera, a histologija je pokazala veću celularnost i održavanje tkivne strukture.
- Circulišući ljudski albumin bio je značajno viši u grupi sa mikrosferama i ostao povišen do osme nedelje.
- Prisustvo fibroblasta stabilizovalo je hepatocite u agregatima — povećana je ekspresija markera zrelih hepatocita (arginase‑1), sekrecija albumina i aktivnost CYP3A4 posle indukcije rifampicinom.
- Minimalna ćelijska smrt u graftovima (<1.2% TUNEL‑pozitivnih), što ukazuje na dobru preživljavanje ćelija u ovoj konfiguraciji.
Uloga degradabilnosti i ultrazvuk
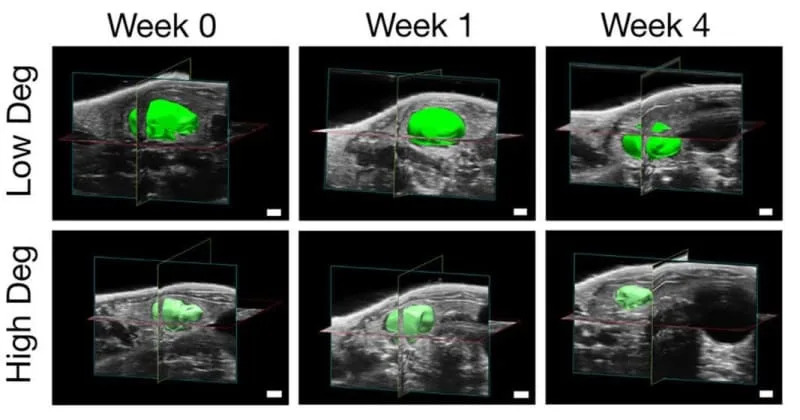
Istraživači su napravili varijante visokogradabilnih i niskogradabilnih mikrosfera. Visokogradabilne su izgubile detektabilnu zapreminu do četvrte nedelje i pokazale remodelovanje niše sa većim lumenima krvnih sudova — što je korelisalo sa većom sekrecijom albumina u četvrtoj nedelji. Niskogradabilne su duže zadržale strukturu, a sudovi su ostali uglavnom unutar praznina.
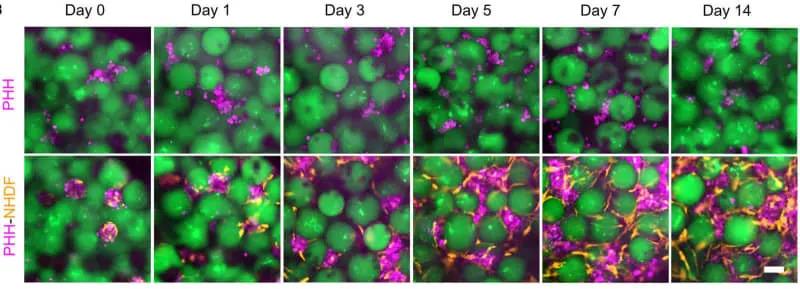
Procedura je razvijena uz ultrazvučno vođeno ubrizgavanje — ultrazvuk je omogućio precizno pozicioniranje i praćenje grafta. Kontrastni ultrazvuk sa mikroboblicama pokazao je perfuzione signale unutar grafta, što potvrđuje vaskularnu povezanost.
Ograničenja i naredni koraci
Autori ističu nekoliko važnih izazova pre kliničke primene: skaliranje (koliko veliku nišu pristup može podržati), snabdevanje adekvatnog broja zrelih hepatocita (stem‑ćelom izvedene ćelije često nisu potpuno zrele), i prevođenje nalaza iz imunodeficijentnog miša u sisteme sa kompletnim imunitetom. Takođe, ultrazvuk dobro detektuje mikrosfersku strukturu, ali ne razlikuje jasno mikrosfere od samih ćelija — buduće verzije mogu imati zasebne kontrastne oznake za svaku komponentu.
Klinički značaj
Ako se pristup uspešno prevede na ljude, injektabilne satelitske niše mogle bi postati minimalno invazivna opcija za pacijente kojima je potrebna kratkoročna ili dopunska podrška jetre — na primer, kao „most“ do transplantacije ili kao alternativna terapija za one koji ne podnose velike operacije. Metoda nije ograničena na jetru i mogla bi da posluži i za druge ćelijske terapije, poput transplantacije ostrvaca pankreasa.
Rad je dostupan u časopisu Cell Biomaterials, vodeći autor studije je Vardhman Kumar.
Pomozite nam da budemo bolji.



























