Ključni rezultat: COLBOS mutacija pojačava vezivanje proteina reelin za heparan sulfat i time lokalizuje reelin na površini neurona, što usporava fosforilaciju tau proteina i nakupljanje amiloida. Posledica: kod nosilaca PSEN1 mutacije početak bolesti je odložen za više decenija. Implikacije: ciljane terapije koje imitiraju ovaj mehanizam (lekovi ili genska terapija) mogle bi značajno produžiti period nezavisnog života.
Jedna genska varijanta reelin‑a može decenijama odložiti Alchajmer — novi uvidi i terapijske perspektive

Novo istraživanje otkriva zašto posebna genska varijanta nazvana COLBOS snažno štiti mozak kod osoba koje su genetski predodređene za rani početak Alchajmerove bolesti. Varijanta utiče na funkciju proteina reelin, koji pomaže neuronima da uklone štetne supstance poput amiloidnih plakova i toksičnih tau čvorova. Rezultat: reelin postaje efikasniji u sprečavanju ključnih procesa bolesti i lokalizuje se na površini neurona gde njegove zaštitne funkcije najviše znače.
Poreklo otkrića: kolumbijska populacija i PSEN1
Priča počinje u dolinama oko Medellína u Kolumbiji, gde je neurolog dr Francisco Lopera decenijama mapirao porodice sa retkom, autosomno dominantnom mutacijom u genu PSEN1. Nosilac te mutacije gotovo sigurno razvija Alchajmer u srednjim četrdesetim. Lopera je otkrio jedan izuzetak: pacijenta sa PSEN1 mutacijom koji je bolest razvio tek u šezdesetim godinama. Iza te otpornosti stajao je drugi genetski faktor — COLBOS.
Kako COLBOS menja funkciju reelina
Studija objavljena u decembru 2025. u Journal of the American Chemical Society (autori uključuju Chunyu Wanga i saradnike sa Rensselaer Polytechnic Institute) pokazuje mehanizam zaštite. COLBOS menja interakciju reelina sa heparan sulfatom — šećernim molekulom na površini ćelija. Korišćena je tehnika surface plasmon resonance (SPR) koja je pokazala da COLBOS pojačava vezivanje reelina za heparan sulfat, delujući kao „molekularni lepak" koji pomaže reelin‑u da ostane na površini neurona.
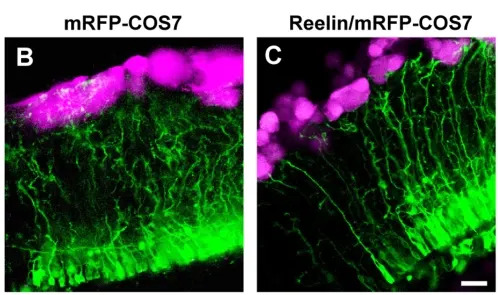
Na toj površini reelin efikasnije pokreće signalne puteve koji smanjuju fosforilaciju tau proteina i ograničavaju nagomilavanje amiloida — ključne procese u razvoju neurodegeneracije.
Granice zaštite i biološki kontekst
Stručnjaci, među kojima je i dr Joachim Herz, ukazuju da COLBOS uglavnom odlaže, a ne potpuno sprečava bolest. Kod nosilaca PSEN1 mutacije postoje kvarovi u endolizosomskim sistemima — ćelijskim „drobilicama" koje razgrađuju štetne proteine. COLBOS poboljšava dostavljanje tih proteina u endolizozome, ali kako mozak stari, problemi u tim organelama postaju teži za prevazilaženje, pa bolest na kraju napreduje.
Terapijske implikacije
Nalazi otvaraju dve glavne mogućnosti: 1) razviti lekove koji pojačavaju vezivanje reelina za heparan sulfat ili stabilizuju njegove efekte na površini neurona, i 2) genske terapije koje pojačavaju reelin signalizaciju. Wang i saradnici već raspravljaju o razvoju genske terapije zasnovane na ovim otkrićima. Autori naglašavaju da i delimično odlaganje bolesti za nekoliko godina ima veliku vrednost; COLBOS je u slučaju kolumbijskih pacijenata odložio pojavu simptoma za oko 20 godina, mnogo više nego postojeće terapije.
„Da sam mi rekao da će varijanta biti toliko zaštitna da može poništiti efekat dominantne PSEN1 mutacije, ne bih verovao," rekao je dr Joachim Herz za Live Science.
Zaključak
Otkrivanje mehanizma kojim COLBOS menja funkciju reelina predstavlja značajan korak ka razumevanju i potencijalnom lečenju Alchajmerove bolesti. Iako je nalaz zasnovan na retkom genetskom modelu (nosilac PSEN1), isti princip — pojačavanje reelinove funkcije na površini neurona — može imati širu primenu u terapijama za klasični, sporije napredujući Alchajmer.
Pomozite nam da budemo bolji.























