MIT tim je razvio mali podkožni implant sa ugrađenim generatorom kiseonika koji je održao funkciju transplantovanih ćelija za proizvodnju insulina kod glodara do 90 dana bez imunosupresije. Uređaj razdvaja vodenu paru na kiseonik i vodonik, pri čemu kiseonik hrani ostrvca, a napajanje se vrši bežično preko spoljne antene. Preliminarni rezultati na majmunu posle jednog meseca nisu pokazali imunološko odbacivanje, ali su potrebne duže i obimnije studije zbog izazova poput fibroze oko implanta i potrebe za dužim preživljavanjem ćelija.
Mali podkožni implant koji proizvodi kiseonik može zameniti injekcije insulina — normoglikemija kod životinja do 90 dana

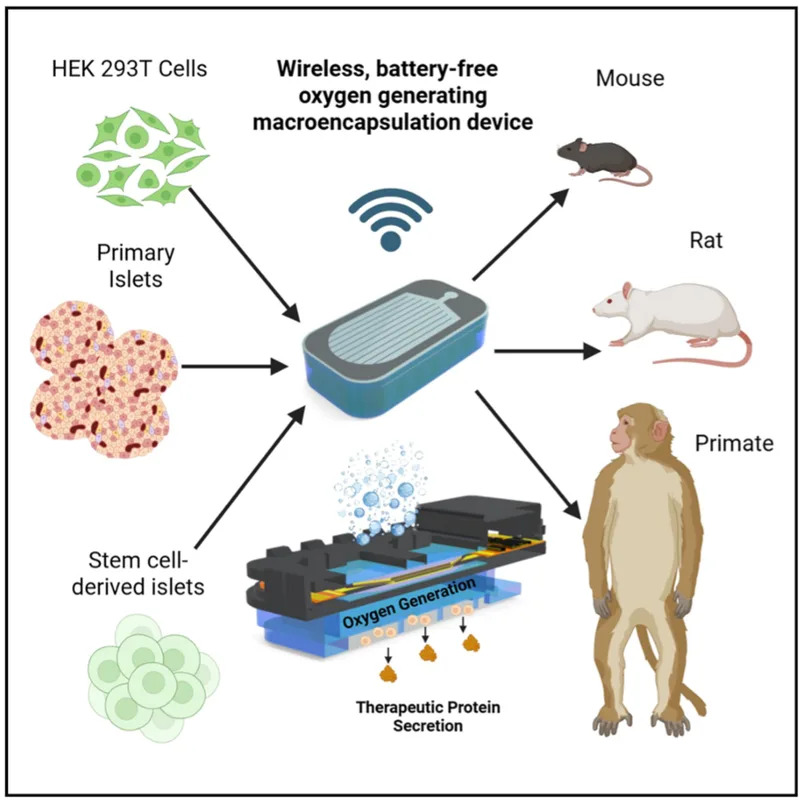
Mali uređaj ugrađen neposredno ispod kože, veličine približno velike poštanske marke i mase oko dva grama, održao je miševe i pacove sa dijabetesom u normoglikemiji do 90 dana bez primene imunosupresivnih lekova. Rezultat, koji su objavili istraživači sa MIT‑a, predstavlja značajan korak ka mogućoj terapiji ćelijama za osobe sa tipom 1 dijabetesa bez dugotrajne imunosupresije.

Kako uređaj funkcioniše
U srcu implanta nalazi se integrisan sistem za proizvodnju kiseonika: protonska membrana koja razdvaja vodenu paru (gasnu fazu H2O) dostupnu u tkivima u vodonik (H2) i kiseonik (O2). Vodonik bezbedno izlazi iz uređaja, dok se kiseonik skladišti u unutrašnjem rezervoaru i difuzijom napaja komoru sa transplantovanim pankreasnim ostrvcima (islets). Uređaj se bežično napaja preko spoljne antene postavljene na kožu, što eliminiše potrebu za kablovima.
Rezultati istraživanja
Tim je testirao tri eksperimentalna modela: miševe sa donorskim ostrvcima, miševe sa ostrvcima izvedenim iz matičnih ćelija i pacove sa modularno povezana dva uređaja. U modelu sa donorskim ostrvcima životinje su održavale normalan nivo glukoze do 90 dana dok su uređaji bili implantirani; po vađenju implanta glikemija se vratila na pred‑transplantacione vrednosti, što potvrđuje ulogu ugrađenih ćelija u kontroli glukoze. Kod modela sa ćelijama iz matičnih ćelija kontrola glikemije je bila slabija, što autori pripisuju vrstnim razlikama i potrebnom vremenu dozrevanja ćelija nakon transplantacije.
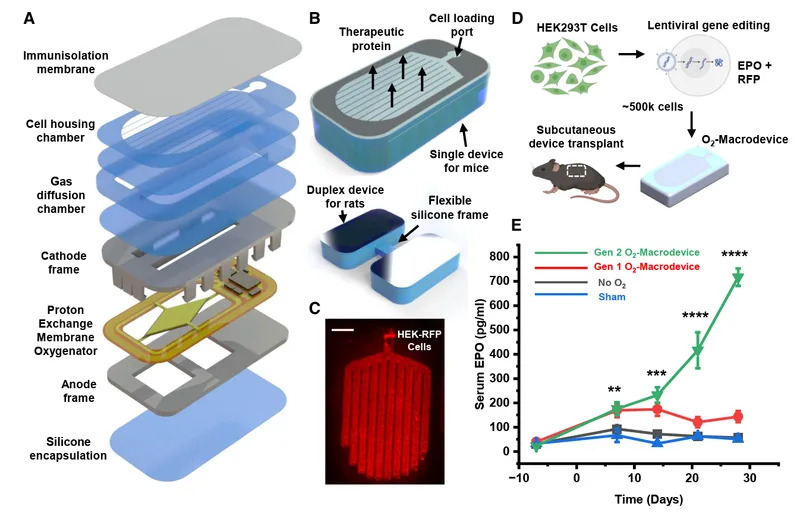
Uvećana snaga i poboljšana vodootpornost nove iteracije uređaja omogućile su znatno duži rad u odnosu na ranije verzije koje su radile oko mesec dana. Modularni pristup je pokazao i dodatnu pouzdanost — ako jedan modul zakaže, drugi može nastaviti da radi.
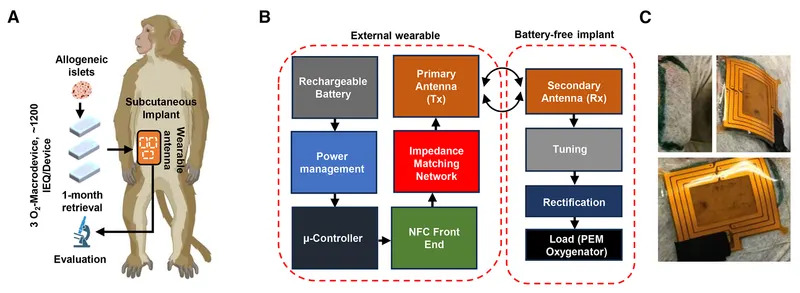
Preliminarni podaci na primatu i ograničenja
U preliminarnoj studiji na cinomolgus majmunu implant je pratio prenosni sistem antene kroz specijalnu jaknu; nakon jednog meseca ugrađene ćelije su bile vitalne i nisu pokazivale znakove imunog odbacivanja. Ipak, autori naglašavaju da je uzorak malen i da je period kratak, te su potrebne duže i opsežnije studije pre kliničkih ispitivanja kod ljudi.
Glavni izazovi uključuju formiranje fibroznog tkiva oko implanta koje usporava razmenu glukoze i insulina, sporiju reakciju na glukozni test u poređenju sa zdravim kontrolama, kao i potrebu za većom gustinom ćelija i dužim preživljavanjem grafta. Neke životinje su uginule tokom studije, ali istraživači navode da su uzroci uglavnom bili povrede usled sukoba ili komplikacije povezane sa nekontrolisanim dijabetesom u kontrolnim grupama, a ne toksičnost uređaja.
Praktičan značaj i naredni koraci
Ako se pristup pokaže bezbednim i efikasnim kod ljudi, implant koji obezbeđuje kiseonik i zaštitu ćelija bez sistemske imunosupresije mogao bi značajno smanjiti teret svakodnevne primene insulina i monitoringa kod osoba sa tipom 1 dijabetesa. Tim trenutno radi na produženju preživljavanja transplantovanih ostrvaca do ciljanih dve godine i razmatra primenu platforme i za druge bolesti koje zahtevaju stalnu ili ponovljenu isporuku proteina, enzima ili antitela.
Napomena: Istraživanje je i dalje u ranoj fazi. Potrebne su duže studije na većim životinjskim modelima i rigorozna ispitivanja bezbednosti pre nego što se razmotre klinički pokušaji na ljudima.
Pomozite nam da budemo bolji.