Naučnici sa University of York identifikovali su protein ESB2 koji deluje kao "molekularni drobilac" i omogućava Trypanosoma brucei da selektivno razgrađuje RNA pomoćnih proteina, pružajući prioritet proizvodnji zaštitnog VSG omotača. Genetsko uklanjanje ESB2 dovelo je do porasta nivoa drugih proteina, čime je potvrđena njegova uloga. Otkriće otvara nove putove za razvoj terapija, a rezultati su objavljeni u Nature Microbiology.
Otkriven "Molekularni Drobilac" ESB2: Kako Trypanosoma brucei Varaju Imuni Sistem

Naučnici sa University of York otkrili su protein koji pomaže parazitu Trypanosoma brucei da godinama prolazi neopaženo kroz imuni sistem. Novi molekul, nazvan ESB2, deluje kao selektivni "molekularni drobilac" RNA i objašnjava dugogodišnju misteriju o tome kako parazit održava svoj zaštitni omotač bez ugrožavanja drugih ćelijskih procesa.
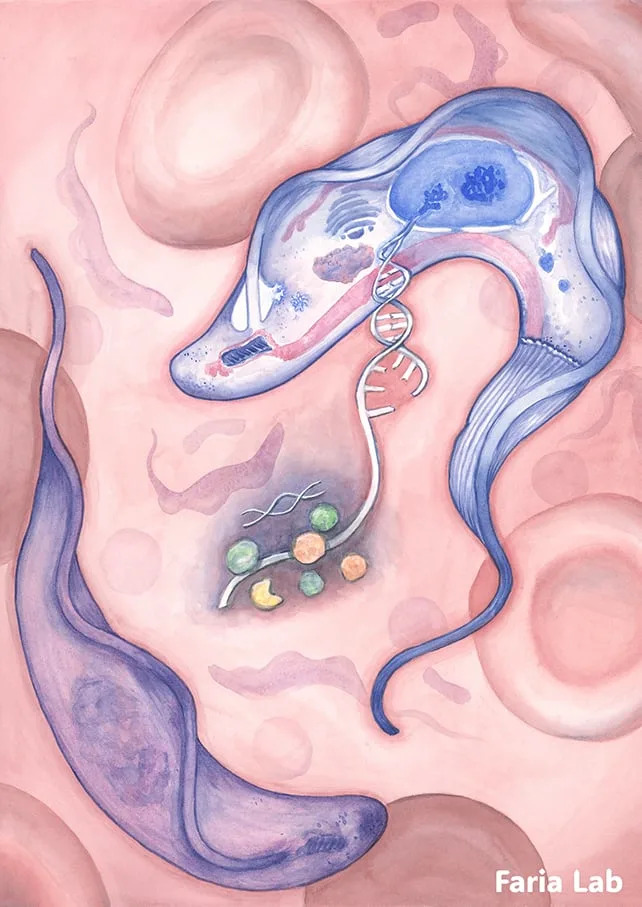
Šta su istraživači otkrili?
Trypanosoma brucei štiti se stalnom obnovom varijantnog površinskog glikoproteina (VSG), sloja koji maskira parazita od imunog sistema. Tim je otkrio da ESB2 omogućava prolaz RNA koja kodira VSG, dok istovremeno razgrađuje (degraduje) RNA za pomoćne proteine. Na taj način se prioritet daje proizvodnji VSG bez nepotrebnog opterećenja proizvodnih kapaciteta ćelije.

"Kada smo prvi put videli molekularni drobilac pod mikroskopom, znali smo da smo otkrili nešto posebno", kaže mikrobiološkinja Lianne Lansink, prva autorka studije.
Kako su došli do otkrića?
Istraživači su obeležili proteine u ćelijama parazita i identifikovali ih masenom spektrometrijom. Nakon identifikacije ESB2, genetski su izmenili T. brucei tako da protein uklone. U odsustvu ESB2, nivoi pomoćnih proteina su porasli i izjednačili se sa nivoima VSG, čime je potvrđena uloga ESB2 u selektivnoj degradaciji RNA.

"Zamislite molekularni drobilac u genetskoj štampariji koji briše određene stranice dok se štampaju", objašnjava prof. Joana Correia Faria, starija autorka studije. "To je efikasan način utišavanja gena na izvoru."
Šta ovo znači za lečenje?
Otkrivanje ESB2 otvara novu potencijalnu metu za terapije: inhibicija ovog proteina mogla bi da omogući imunom sistemu da prepozna parazita ili da oslabi njegovu sposobnost za maskiranje. Ipak, razvoj lekova je i dalje u ranoj fazi i zahteva dodatna istraživanja kako bi se proverila bezbednost i efikasnost takvih pristupa.
Kontekst bolesti
Spavaća bolest (afrička tripanosomijaza) prenosi se ujedom tsetse muve i utiče na centralni nervni sistem — izazivajući poremećaje sna, konfuziju, pa i komu. Broj obolelih je smanjen tokom poslednjih godina, ali bolest i dalje pogađa stotine ljudi godišnje u endemskim oblastima, a postojeći tretmani nisu uvek dostupni i mogu imati ozbiljne neželjene efekte.
Rad je objavljen u časopisu Nature Microbiology. Istraživači planiraju dalje da proučavaju kako ESB2 razlikuje različite RNA molekule i koje proteine koristi u tom procesu.
Pomozite nam da budemo bolji.