Studija EPFL-a pokazuje da kratka, ciljano kontrolisana ekspresija faktora Oct4, Sox2 i Klf4 (OSK) u engram neuronima može povratiti učenje i udaljena sećanja kod starih miševa i u modelima Alchajmerove bolesti. OSK obnavlja markere neuronskog identiteta i heterohromatinske karakteristike, vraća neke gene i pristupačnost hromatina prema mlađem profilu i normalizuje neuronalnu ekscitabilnost. Iako su rezultati ohrabrujući, ostaju pitanja bezbednosti i trajnosti efekata.
Ciljano „Pomlađivanje” Neurona Vraća Pamćenje kod Starih i Alchajmerovih Miševa

Starenje i neurodegenerativne bolesti često narušavaju sposobnost mozga da sačuva i prizove sećanja. Nova studija grupe Johannesa Gräffa (EPFL, Brain Mind Institute), objavljena u časopisu Neuron, pokazuje da kratka i ciljano kontrolisana ekspresija faktora Oct4, Sox2 i Klf4 (OSK) u neuronima koji nose konkretno sećanje (tzv. engram ćelije) može vratiti učenje i daleka (remote) sećanja kod starih miševa i u modelima Alchajmerove bolesti.
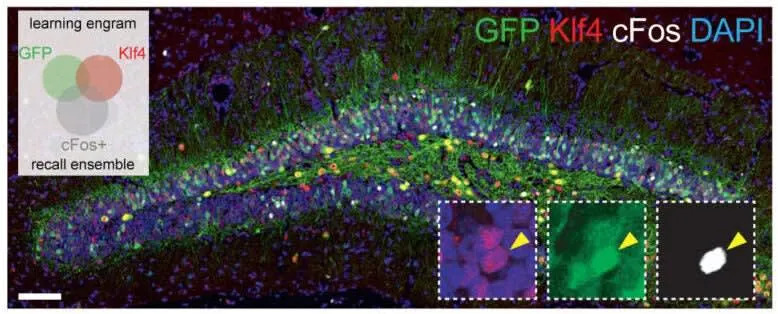
Šta su engrami i kako je primenjen OSK?
Engrami su retke grupe neurona koje se aktiviraju tokom učenja i kasnije učestvuju u prizivanju tog sećanja. Istraživači su koristili kombinovani sistem: c-Fos bazirano označavanje neurona aktiviranih tokom učenja i tet-regulisan vektor za kratku indukciju OSK (tet-off sistem, kontrolisan doksiciklinom). Tako su OSK faktori uključivani samo u ćelije koje su aktivne u vremenskom prozoru učenja, a zatim brzo gašeni.
Regije fokusirane u studiji
Intervencije su bile ciljane na dve ključne regije:
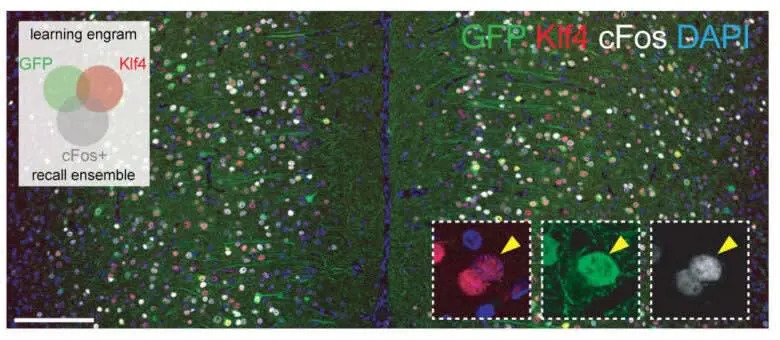
- Dentatni girus (DG) hipokampusa – bitan za učenje i nedavno prizivanje.
- Medijalna prefrontalna kora (mPFC) – važna za udaljeno (remote) pamćenje.
Behavioralni rezultati
U zadatku kontekstualnog učenja straha, stari miševi (9–10 meseci) pokazali su smanjeno zamrzavanje i lošiju reaktivaciju DG engrama u odnosu na mlade. Kada je OSK ciljano induciran u DG engramima, pamćenje starijih miševa vraćeno je na nivo mladih. Slično, kratka OSK indukcija u mPFC-u spasila je udaljeno prizivanje dve nedelje posle učenja.
Modeli Alchajmerove bolesti
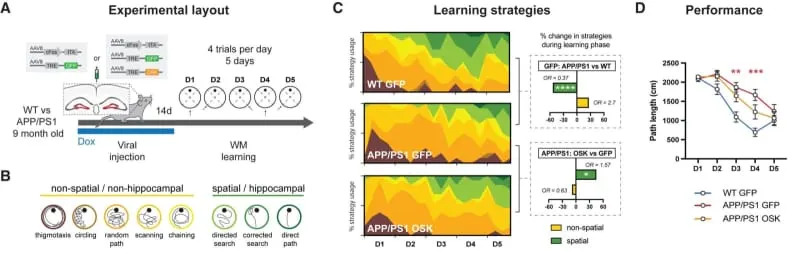
U APP/PS1 miševa (amiloidni AD model) OSK u DG je poboljšao upotrebu hipokampalnih navigacionih strategija tokom treninga u Morrisovom vodićem labirintu, a ciljano reprogramiranje mPFC engrama dovelo je do oporavka udaljenog prostornog pamćenja dve nedelje kasnije. Kontrola je pokazala da efekt zavisi od toga da je OSK tačno ciljano na ćelije koje su sudelovale u učenju — ne pomaže ako se OSK uključi u ćelije aktivirane pri istraživanju novog okruženja.
Molekularni, hromatinski i elektrofiziološki nalazi
- Single-nucleus multiome (snRNA-seq + snATAC-seq) u mPFC pokazao je da APP/PS1 engrami gube ekspresiju gena identiteta i engram potpise, što je delom ili potpuno vraćeno OSK tretmanom.
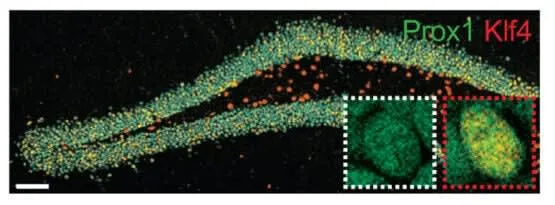
- OSK je povećao ekpresiju markera neuronskog identiteta (npr. Prox1 u DG, Ctip2 u dubljim slojevima mPFC), i obnovio heterohromatinske i nuklearne karakteristike povezane sa mlađim ćelijama (H3K9me3, LaminB1, kružnost jedra).
- Promene u pristupačnosti hromatina bile su složenije: mnoge AD-povezane promene su se vratile, a OSK je naročito izazvao dobitke u distalnim regijama obogaćenim za Klf4 motive (primer: Kcnj3/Kir3.1).
- Elektrofiziologija: engram neuroni u APP/PS1 su bili hipereksitabilni (više AP pri istoj injekciji struje, manji reobaz). OSK je normalizovao ekscitabilnost, a aktivator Kir3.1 (ML-297) je opet efikasno hiperpolarizovao reprogramirane ćelije, što ukazuje na vraćanje funkcije Kcnj3/Kir3.1.
Kognitivni "sat" i trajnost efekata
Istraživači su koristili regresioni model ponašanja u vodićem labirintu da predvide hronološki uzrast ("kognitivni sat"). OSK je smanjio predviđeni biološki uzrast kod starih i AD modela miševa, što podržava ideju o funkcionalnom pomlađivanju obrazaca učenja. Međutim, trajanje efekata van ispitivanog perioda (do dve nedelje) još nije poznato.
Ograničenja i bezbednost
Autori navode nekoliko ograničenja: korišćenje amiloidnih (ne tau) modela AD, analiza u jednoj tački posle dve nedelje, fokus na mPFC ekscitatorne engrame i mogućnost da u sekvenciranju postoji mali udeo nereprogramiranih ćelija koji razvodnjava efekte. Važno je i napomenuti rizike reprogramiranja (opasnost od de-diferencijacije ili tumora) ako se faktori OSK ne kontrolišu striktno — u studiji je dizajn imao ciljani i kratak vremenski prozor kako bi se umanjili ti rizici.
Zaključak
Rad pokazuje da ciljano, parcijalno reprogramiranje memorijskih engram ćelija može vratiti molekularnu, funkcionalnu i ponašajnu komponentu pamćenja kod starenja i u amiloidnim modelima Alchajmera. To otvara novu strategiju — ne popravljanje celog mozga, već obnavljanje ćelija koje konkretno čuvaju određenog sećanja — ali ostaju važna pitanja o sigurnosti, mehanizmima i trajanju efekata pre bilo kakvog prevođenja na ljude.
Izvor: Gräff i saradnici, Neuron; EPFL Brain Mind Institute.
Pomozite nam da budemo bolji.