Nova studija identifikovala je protein NR2F1 kao ključni uzrok fibrotičnih ožiljaka i zamagljenja sočiva posle operacije katarakte. Kvar autofagije dovodi do nakupljanja NR2F1, koji aktivira STAT3 i pokreće EMT, fibrozu i apoptozu. Utišavanje NR2F1 ili blokada STAT3 u ćelijskim i mišjim modelima smanjili su ožiljke i sačuvali providnost leće, ali su potrebna dalja istraživanja pre primene na ljudima.
Zašto se pojavljuju ožiljci posle operacije katarakte? Novi uvid u ulogu NR2F1 i STAT3

Katarakta ostaje jedan od najčešćih uzroka gubitka vida u svetu. Iako operacija često povrati vid, kod mnogih pacijenata se kasnije javljaju fibrotični ožiljci ispod kapsule sočiva koji ponovo zamagle vid i ograniče oporavak. Nova studija koju su predvodili naučnici sa Chongqing Medical University i Chongqing General Hospital objašnjava molekularne mehanizme koji stoje iza ovog problema i ukazuje na potencijalne terapijske pristupe.
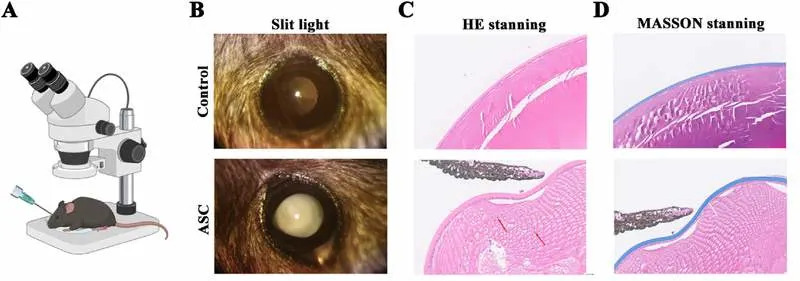
Istraživanje identifikovalo je protein NR2F1 kao ključni pokretač oštećenja ćelija sočiva i fibrotičnog ožiljavanja. Autori pokazuju da kvar u ćelijskom sistemu za reciklažu — autofagiji — dovodi do nakupljanja NR2F1, što zatim aktivira signalni put STAT3. Aktiviran STAT3 podstiče epitelnomezenhimalnu tranziciju (EMT), fibrozne promene i apoptozu, što dovodi do formiranja zamagljenih, fibrotičnih plakova ispod kapsule sočiva.
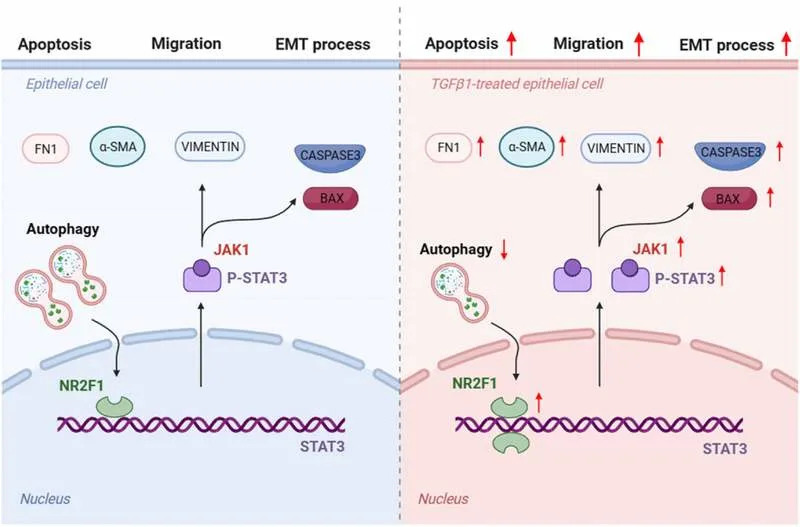
„Naša studija otkriva ključnu vezu između disfunkcije autofagije i formiranja fibrotične katarakte“, rekao je prof. Wenjuan Wan. „Identifikacijom NR2F1 kao direktnog aktivatora STAT3 puta, otkrili smo mehanizam koji pokreće fibrozu sočiva i smrt ćelija.“
Ključni eksperimentalni nalazi:
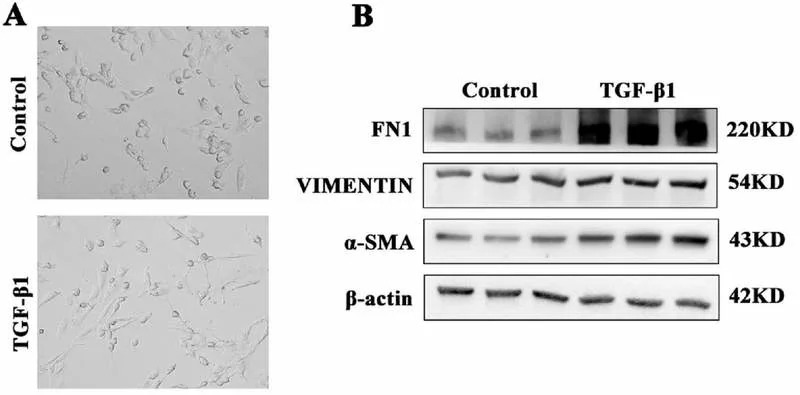
- U ćelijama sočiva izloženim TGF‑beta autofagija se usporava, dok se NR2F1 protein nakuplja unutar ćelija. Zanimljivo, nivo NR2F1 mRNA se smanjuje, što ukazuje na to da je problem u uklanjanju proteina, a ne u prekomernoj sintezi.
- Direktno blokiranje autofagije dovelo je do dodatnog porasta NR2F1, potvrđujući vezu između kvarova u „ćelijskom čišćenju“ i akumulacije proteina.
- NR2F1 se vezuje za kontrolni region gena STAT3 i aktivira ga, čime se pokreću signalne kaskade koje podstiču EMT, migraciju ćelija, fibrozne promene i programiranu smrt ćelija.
- U laboratorijskim uslovima utišavanje NR2F1 smanjilo je EMT, fibrotične markere i migraciju ljudskih ćelija sočiva, dok su u miševima tretmani koji utišavaju NR2F1 (adeno‑asocirani virus, AAV) ili inhibitori STAT3 smanjili formiranje fibroznih plakova i sačuvali providnost leće.
Šta to znači za pacijente i lečenje
Otkriveni put (autofagija → NR2F1 → STAT3 → EMT/fibroza/apoptoza) nudi novi cilj za lekove koji bi mogli da spreče ili ublaže ožiljke posle operacije katarakte. Takve terapije bi mogle da:
- smanje potrebu za ponovnim hirurškim intervencijama,
- poboljšaju i produže rezultate zamene sočiva,
- omoguće zaštitu vida u oblastima sa ograničenim pristupom hirurgiji.
Ograničenja i dalje potrebne studije
Iako su rezultati u ćelijskim i životinjskim modelima obećavajući, potrebne su dodatne studije o bezbednosti, optimalnom vremenu primene i načinima isporuke u ljudima. Terapije koje koriste AAV ili hemijske inhibitore zahtevaju opsežno testiranje pre kliničke i kliničke primene.
Studija takođe otvara pitanja o ulozi NR2F1 i STAT3 u drugim fibrotičnim bolestima i raku, jer su oba proteina implicirana u fibrogenim procesima u više tkiva.
Zaključak: Rad pruža čvrst molekularni okvir koji objašnjava kako disfunkcija autofagije može dovesti do fibrotične katarakte i identifikuje NR2F1/STAT3 kao atraktivne terapeutske mete. Objavljeno u časopisu Genes & Diseases, istraživanje je važan korak ka lekovima koji bi mogli smanjiti zavisnost od operacije i poboljšati dugoročne ishode za pacijente.
Pomozite nam da budemo bolji.